Tofacitinib citrate ialah ubat preskripsi (nama dagangan Xeljanz) yang pada asalnya dibangunkan oleh Pfizer untuk kelas perencat Janus kinase (JAK) oral. Ia secara terpilih boleh menghalang JAK kinase, menyekat laluan JAK/STAT, dan dengan itu menghalang transduksi isyarat sel dan ekspresi dan pengaktifan gen yang berkaitan, digunakan untuk merawat arthritis rheumatoid, arthritis psoriatik, kolitis ulseratif dan penyakit imun yang lain.
Ubat ini termasuk tiga bentuk dos: tablet, tablet pelepasan berterusan dan penyelesaian oral. Tabletnya pertama kali diluluskan oleh FDA pada tahun 2012, dan borang dos pelepasan berterusan telah diluluskan oleh FDA pada Februari 2016. Ia adalah yang pertama untuk merawat sendi reumatoid. Yan adalah perencat JAK yang diambil secara lisan sekali sehari. Pada Disember 2019, petunjuk baharu untuk ubat pelepasan berterusan telah diluluskan sekali lagi untuk kolitis ulseratif (UC) aktif sederhana hingga teruk. Di samping itu, ujian klinikal fasa 3 semasa untuk psoriasis plak telah selesai, dan enam lagi ujian klinikal fasa 3 sedang dijalankan, melibatkan arthritis psoriatik aktif, arthritis idiopatik juvana, dsb. Jenis petunjuk. Kelebihan tablet sustained-release yang tahan lama dan hanya perlu diambil sekali sehari adalah kondusif untuk pengurusan dan kawalan penyakit pesakit.
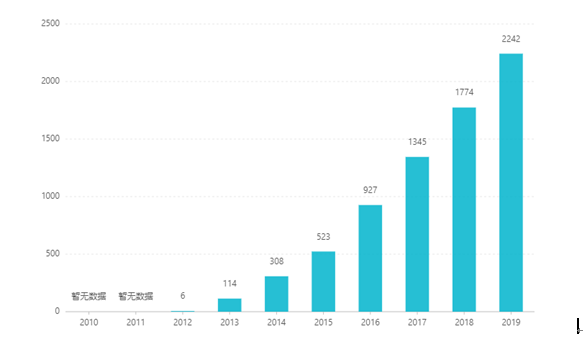
Sejak penyenaraiannya, jualannya meningkat tahun demi tahun, mencecah AS$2.242 bilion pada 2019. Di China, borang dos tablet telah diluluskan untuk pemasaran pada Mac 2017, dan memasuki katalog insurans perubatan kategori B melalui rundingan pada 2019. Kemenangan terbaru tawaran ialah RMB 26.79. Walau bagaimanapun, disebabkan halangan teknikal yang tinggi bagi persediaan pelepasan berterusan, bentuk dos ini belum lagi dipasarkan di China.
JAK kinase memainkan peranan penting dalam keradangan, dan perencatnya telah ditunjukkan untuk merawat penyakit keradangan dan autoimun tertentu. Sehingga kini, 7 perencat JAK telah diluluskan di seluruh dunia, termasuk Delgocitinib Leo Pharma, Fedratinib Celgene, upatinib AbbVie, Pefitinib Astellas, Baritinib Eli Lilly dan Rocotinib Novartis. Walau bagaimanapun, hanya tofacitinib, baritinib dan rocotinib yang diluluskan di China antara ubat-ubatan yang disebutkan di atas. Kami berharap "Tablet Pelepasan Berkekalan Tofatib Citrate" Qilu diluluskan secepat mungkin dan memberi manfaat kepada lebih ramai pesakit.
Di China, penyelidikan asal tofacitib sitrat telah diluluskan oleh NMPA pada Mac 2017 untuk rawatan pesakit RA dewasa dengan keberkesanan atau intoleransi yang tidak mencukupi untuk methotrexate, di bawah nama dagang Shangjie. Menurut data daripada Meinenet, jualan tablet tofacitib sitrat di institusi perubatan awam China pada 2018 ialah 8.34 juta yuan, yang jauh lebih rendah daripada jualan globalnya. Sebahagian besar sebabnya ialah harga. Dilaporkan bahawa harga runcit awal Shangjie ialah 2085 yuan (5mg*28 tablet), dan kos bulanan ialah 4170 yuan, yang bukan beban kecil untuk keluarga biasa.
Walau bagaimanapun, adalah wajar untuk meraikan bahawa tofacitib telah dimasukkan ke dalam "Insurans Perubatan Asas Kebangsaan, Insurans Kecederaan Kerja dan Senarai Ubat Insurans Bersalin" 2019 oleh Pentadbiran Insurans Perubatan Kebangsaan selepas rundingan pada November 2019. Dilaporkan bahawa yuran bulanan akan dikurangkan kepada di bawah 2,000 yuan selepas pemotongan harga dirundingkan, yang akan meningkatkan ketersediaan ubat.
Pada Ogos 2018, Lembaga Peperiksaan Semula Paten Pejabat Harta Intelek Negeri membuat keputusan semakan No. 36902 permintaan untuk pembatalan, dan mengisytiharkan tidak sah paten teras Pfizertofatib, paten kompaun, atas alasan penzahiran spesifikasi yang tidak mencukupi. Walau bagaimanapun, paten bentuk kristal Pfizertofatiib (ZL02823587.8, CN1325498C, tarikh permohonan 2002.11.25) akan tamat tempoh pada 2022.
Pangkalan data Insight menunjukkan bahawa, sebagai tambahan kepada penyelidikan asal, lima ubat generik Chia Tai Tianqing, Qilu, Kelun, Sungai Yangtze dan Nanjing Chia Tai Tianqing telah diluluskan untuk pemasaran dalam formulasi tablet tofacitinib domestik. Walau bagaimanapun, untuk jenis tablet keluaran berterusan, hanya penyelidikan asal Pfizer yang mengemukakan permohonan pemasaran pada 26 Mei. Qilu ialah syarikat domestik pertama yang mengemukakan permohonan pemasaran untuk formulasi ini. Selain itu, CSPC Ouyi berada dalam peringkat percubaan BE.
Kilang Farmaseutikal Changzhou (CPF) ialah pengeluar farmaseutikal terkemuka bagi API, menyiapkan formulasi di China, yang terletak di Changzhou, wilayah Jiangsu. CPF telah diasaskan pada tahun 1949. Kami telah mengabdikan diri dalam Tofacitinib Citrate dari 2013, dan telah pun menyerahkan DMF. Kami telah mendaftar di banyak negara, dan boleh menyokong anda dengan sokongan dokumen terbaik untuk Tofacitinib Citrate.
Masa siaran: Jul-23-2021